がん治療は、細胞の増殖や増殖機構を広く標的とする非特異的な細胞障害性薬剤を用いた従来型治療から、徐々に進化しています。現在では、研究から得られた知見により、患者ごとの腫瘍特異的な分子マーカーに合わせた個別化治療の開発が可能になっています。これには、標的治療につながる可能性を持つ、がんドライバー変異などの創薬可能なゲノム変異が含まれます。予測バイオマーカーに基づく治療は、患者に最適化された標的治療を提供することを目的としたPrecision Oncology(精密腫瘍医療)の基盤を形成しており、個別化医療の分野として進化を続けています。Precision Medicine(精密医療)の長期的なビジョンは、オフターゲットによる副作用を最小限に抑えながら、患者の生存率とQOL(生活の質)を最大化できる最適な治療法を特定することです。
本ブログでは、移行上皮がんとも呼ばれる尿路上皮がん(Urothelial Carcinoma)について取り上げ、近年の研究や発見がどのようにPrecision Medicine(精密医療)の開発や患者のQOL向上に貢献しているかを解説します。尿路上皮がんは、膀胱、尿管、腎盂を含む尿路を覆う尿路上皮細胞から発生することが多いがんです。これは、膀胱がんの中で最も一般的な種類です。主な症状として、血尿、頻尿、排尿時の痛みなどが挙げられます。
治療法は、がんの進行度や発生部位によって異なり、手術、化学療法、放射線療法、免疫療法などが含まれます。より良い治療成績を得るためには、早期発見と早期治療が重要です。World Cancer Research Fundの2022年の報告によると、世界では年間614,298件を超える新規症例が診断され、20万人以上がこの疾患によって死亡しており、世界的に深刻な健康課題となっています。
National Cancer Institute(Surveillance, Epidemiology, and End Results Program)のデータによると、2024年の米国では、膀胱がんの新規症例数は83,190件(全がん症例の4.2%)、死亡者数は16,840人(全がん死亡の2.8%)と推定されており、5年生存率は78.4%とされています。一方で、アジア人集団は特有の遺伝的パターンを有している点で注目されています。 これにより、疾患の生物学的理解に関する重要な知見が得られるとともに、Precision Medicine(精密医療)解析に基づく革新的な治療戦略の可能性が広がっています。
最近のシステマティックレビューでは、アジア人膀胱がん患者におけるFibroblast Growth Factor Receptor 3(FGFR3)のゲノム変異の頻度および臨床的意義について詳しく検討されており、Precision Oncology(精密腫瘍医療)およびバイオインフォマティクス主導型のがん研究における有望な新領域として注目されています。
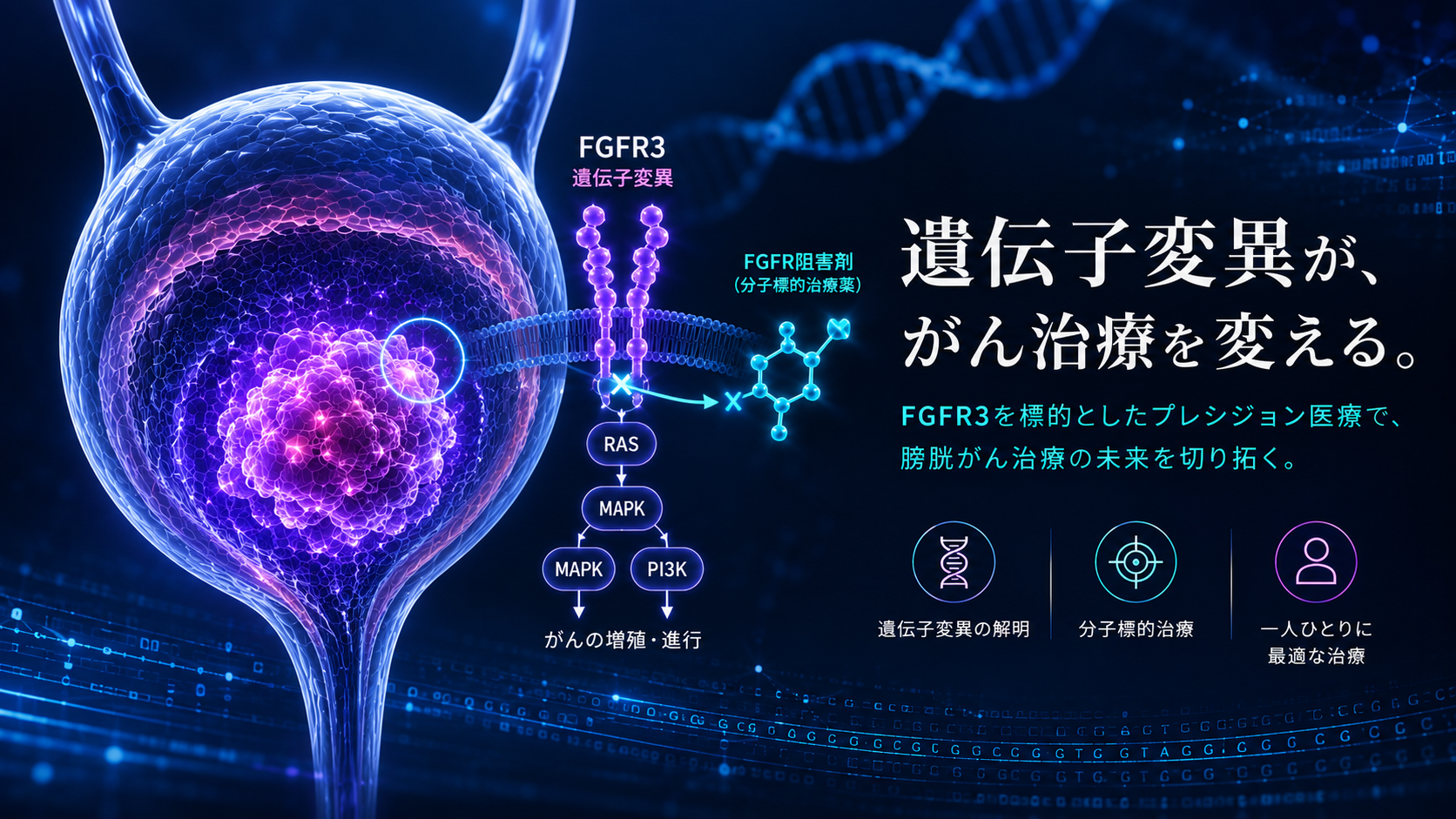
FGFR3:主要ながんドライバーの一つ
FGFR3は膀胱尿路上皮がんにおける重要な遺伝子であり、腫瘍増殖に関与する変異や構造変異が高頻度で認められます。アジア人患者では、ホットスポット変異であるS249C変異を含むFGFR3変異が最大18.4%の症例で確認されており、この集団において一般的な遺伝子変異となっています。これらの変異はTP53変異と相互排他的に存在することが多く、異なる発がん経路の存在を示唆しています。これは、FGFR3が一部の膀胱がん患者において重要ながんドライバーとして機能していることを示しており、データ駆動型創薬およびPrecision Oncology(精密腫瘍医療)戦略を通じた標的治療介入の機会を提供しています。
| 番号 | 国名 | 新規症例数 |
|
1 |
米国 | 80404 |
| 2 |
中国 |
92883 |
| 3 | イタリア | 34580 |
| 4 | 日本 | 34568 |
| 5 | ドイツ | 29035 |
| 6 |
英国 |
23643 |
| 7 | インド | 22538 |
| 8 | スペイン | 21418 |
| 9 | フランス(本土) | 19733 |
| 10 | ロシア | 19352 |
| 合計(グローバル) | 614298 |
表1.世界における膀胱尿路上皮がんの発症数(2022年)
出典:Bladder cancer statistics | World Cancer Research Fund
主要ながんドライバーFGFR3に着目した標的治療介入
FGFR3は、膀胱尿路上皮がんにおいて中心的な役割を担う遺伝子として注目されており、腫瘍増殖を促進する変異や構造変異が高頻度で認められています。Tumor protein p53(TP53)は、がん抑制タンパク質であるcellular tumor antigen p53をコードする遺伝子です。このタンパク質は、細胞周期停止、アポトーシス、細胞老化、DNA修復、代謝変化に関わる遺伝子発現を制御しています(Gene 2014)。がんでは、TP53本来の機能が十分に果たされなくなり、その結果として細胞生存、DNA損傷、細胞増殖が促進されます。P53は、がんにおいて最も高頻度に変異が認められる遺伝子であり、全がんの約半数で変異が確認されています(Genetics Home Reference 2014)。
FGFR3変異はTP53変異と相互排他的に存在することが多く、この排他性は、FGFR3が特定の膀胱がんサブタイプにおいて重要ながんドライバーとして機能していることを示しています。そのため、FGFR3は標的治療介入における有望なターゲットとなっています。
FGFR3変異の臨床的意義
FGFR3遺伝子は、骨格形成をはじめとするさまざまな生物学的プロセスにおいて重要な役割を果たしています。この遺伝子の変異は、骨系統疾患に関連するさまざまな疾患や、一部のがんの発症につながる可能性があります。FGFR3遺伝子の機能や変異を理解することは、標的治療の開発および患者予後の改善において重要です。大きなブレークスルーとなったのは、初の低分子FGFR阻害剤であるErdafitinib(Balversa, Janssen Pharmaceuticals)(図2)が、FGFR3またはFGFR2の遺伝子変異を有する進行性膀胱がんを対象としてFDA承認を取得したことです。
図2:Erdafitinib(出典:PubChem Erdafitinib | C25H30N6O2 | CID 67462786 – PubChem)
図
Erdafitinibの臨床試験では、全奏効率が30%を超え、副作用も管理可能であることが示されており、有望な結果が得られています。これらの結果は、より効果的な治療介入と患者予後の改善への期待を高めています。
Precision Medicine:より良い治療成果への指針
分子プロファイリングは、膀胱がん管理において重要な役割を果たします。FGFR3変異や構造変異を特定することは、標的治療の選択指針となるだけでなく、腫瘍生物学の理解にも役立ちます。
FGFR3変異とTP53変異が相互排他的であることは、単一経路のみを標的とした治療では十分ではない可能性を示唆しており、効果的な個別化治療計画を構築するためには、包括的なゲノム解析が必要であることを強調しています。
FGFR3標的治療の今後の展望
FGFR3標的治療は大きな可能性を示していますが、その潜在能力を最大限に引き出すためには、さらなる研究が必要です。今後注目すべき主な研究領域として、以下が挙げられます。
-
併用療法
FGFR3変異とTP53などの他のゲノム変異との相互作用を解析し、相乗効果を持つ治療戦略の構築を目指すこと。 - 分子診断へのアクセス
アジアのように膀胱がん発症率が高い地域において分子プロファイリングの利用可能性を拡大し、Precision Medicine(精密医療)への公平なアクセスを実現すること。
標的治療の進展を踏まえると、依然として大きな課題の一つは薬剤耐性であり、この耐性を克服するための重要なアンメットニーズが存在しています。そのため、患者ごとのニーズに適した相乗的治療パートナーを明らかにし、患者全体の健康状態への影響を最小限に抑えながら局所的に腫瘍増殖を抑制できる治療法を開発するために、さらなる研究が求められています。
アジア人患者に関する詳細については、「Prevalence and Clinical Significance of FGFR3 Genomic Alterations in Asian Bladder Urothelial Carcinoma: A Systematic Review(Asian Journal of Oncology)」をご参照ください。
関連製品